本來想寫關於流column的文章,開始動筆的時候發現流column前,點TLC片是一個很重要的環節,因此先來跟大家介紹一下如何點TLC片,以及會發生的一點小狀況。
1.TLC片裁切大小
一般來說TLC片會裁切成長5 cm,寬1、1.5、2、3公分,寬切到3公分已經是極限,再寬就不容易放進跑片罐中。
2.跑TLC片(假設我們下了一個反應,我們想知道我們這個反應目前的狀況如何)
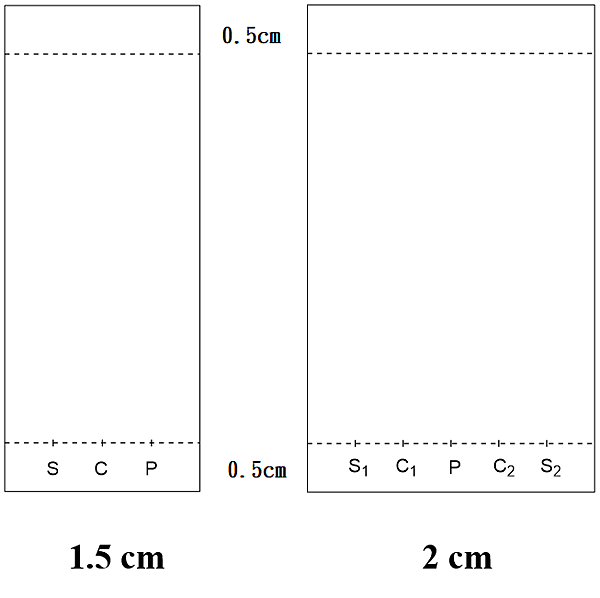
(1)畫TLC片時,下面的線距離底部要空0.5cm,上面的線距離頂部要空0.5cm,如此觀測出來的點的位置是最準確的。
(2)若反應中的起始物只有一個,用1.5 cm的TLC片,點S、C、P三個點
*其中S(sample)=起始物 P(product)點=反應溶液 C(combination)點=起始物和反應溶液點在同一個點上。
(3)若反應中的起始物有兩個,則選用2 cm 的TLC片,點S1、C1、P、C2、S2五個點。
*其中S1=起始物1,C1=起始物1+反應溶液,P=反應溶液,C2=起始物2+反應溶液,S2=起始物2。
接著我們用毛細管將起始物和反應溶液點在TLC片後,丟進跑片罐裡跑片,假設會得到:
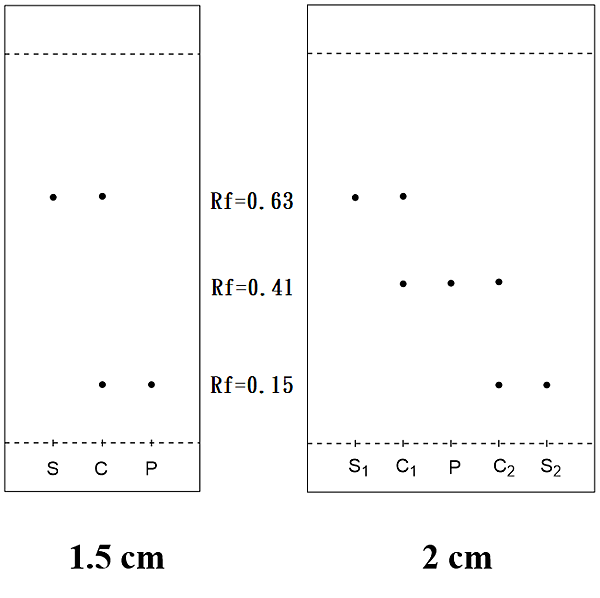
(4)這時我們從1.5cm的TLC片上可看到,起始物的點位於Rf=0.63的位置,而我們尚未純化的溶液(P點)只有一個Rf=0.15的點,這說明了,在反應的過程中我們的起始物完全消耗完畢,並且出現了一個新的化合物(可以收反應了)。
(5)2cm的TLC片同理可知,在P點上只有一個新的點出現,而沒有S1和S2的點,這個時候證明了我們的兩個起始物都消耗完了,並且出現了一個新的化合物。
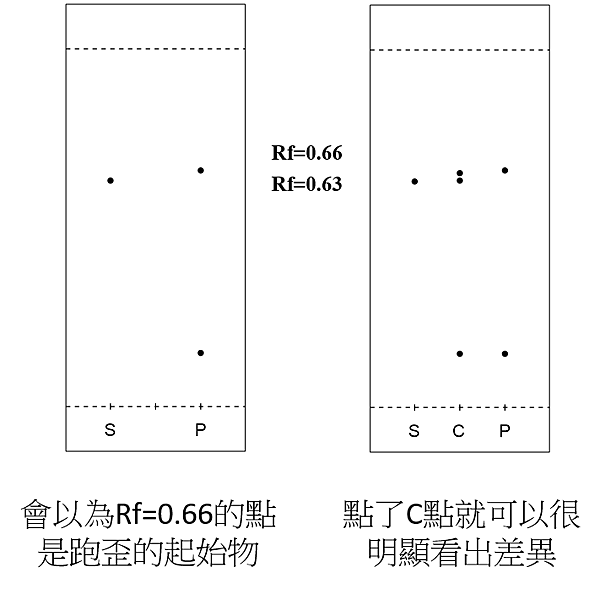
*有些人會疑惑,明明點S和P點就可以看出反應溶液的狀況了,為什麼要點C點呢?因為有時候反應溶液可能會有跟起始物S很相近的點,若我們只點了S和P點,很容易就誤以為它就是S點了。
3.用什麼樣的極性跑TLC片?
(1)每個實驗室慣用的溶劑不同,像我們實驗室最常用的是乙酸乙酯(EA)、正己烷、二氯甲烷(DCM)、乙醚、甲醇,要用甚麼樣的極性去跑,是要自己去嘗試的,試到能清楚看出起始物的消耗狀況,和產物的產生狀況為止。
(2)像我們實驗室通常會使用正己烷(低極性)和乙酸乙酯(高極性)的搭配去跑TLC片,假設從正己烷:乙酸乙酯=5:1開始嘗試的話,跑出來的點太高的話,就降低極性,改用7:1去跑看看;若跑出來的點太低的話,就調高極性,改用3:1去嘗試看看。
(3)不要拘泥於同一種類的溶劑搭配,像我們實驗室通常是使用正己烷和乙酸乙酯搭配,可是如果跑出來的結果不理想的時候,可以更換使用二氯甲烷和乙酸乙酯,或者是二氯甲烷和甲醇……等之類的溶劑搭配,有時候會有出乎意料的結果。
*由於甲醇的極性很大,若用甲醇來搭配的話,甲醇所佔比例不宜過多,否則片上的點容易擴散,不便於觀察。
4.其他跑片時遇到的狀況
(1)若你的反應溶液中含有DMF、DMSO、1,4-dioxane、甲醇、醋酸……等這類不易揮發溶劑,你將反應溶液用毛細管點在TLC片上,跑片前,需要先拿吹風機把TLC片吹一吹,再放到跑片罐跑。原因是這些溶劑不易揮發,極性又大,跑片時很容易帶著你的化合物跑,會呈現擴散的現象,不易觀察,例如:
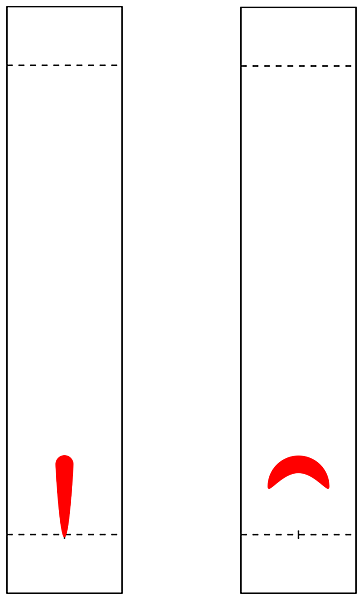
(2)點片時毛細管所吸的溶液濃度太濃,跑完的TLC片上可能會擴散,不利於觀察,要適當稀釋。(好像有點廢話?![]() )
)
(3)若你的反應物,不論用何種溶劑搭配或極性搭配去跑,都在原點的話,就代表你的東西用有機實驗的方法分離不出來。(可以丟了?![]() )
)
(4)TLC片上的silica gel放置在空氣中時,會吸收微量的水氣,若你的目標產物怕水,接觸到水氣容易產生水解,那可能會在跑片的時候受到TLC片中水分的影響,造成我們誤判反應的結果。這個問題可以藉由『烤片』來解決,將TLC片烤一烤(可以下反應加熱時順便放在加熱攪拌器上烤),烤完放置到室溫冷卻一下再點片。
*若不是很清楚TLC片上的水份是否真的會影響到跑片結果,可以烤與未烤的TLC片都各點一張來做對比。
目前只想的到這些,如果有想到其他的再更新上來~




 留言列表
留言列表


